新闻动态
2021年底,美国辉瑞公司的新冠口服药Paxlovid被美国FDA批准上市引发广泛关注。Paxlovid的主要成分之一是代号为PF-07321332的3CL蛋白酶抑制剂。PF-07321332在多种冠状病毒的生命周期中起到重要作用,其潜在优势是对目前所有的新冠病毒变种都可以产生作用,因此该小分子药物吸引了众多医药生产企业的浓厚兴趣。
Paxlovid是一个类似寡肽的药物,其合成步骤涉及多个制备酰胺键的反应(图1)。在倒数第二步制备N-1关键中间体9的时候,生产工艺用EDCl/HOPO作为缩合试剂组合,将3与8两个片段缩合成酰胺键[1]。在这里EDCl起到活化羧酸与缩合脱水的作用,而HOPO起到提高收率并减少消旋副产物的作用(图2)。随着Paxlovid的上市,HOPO这个平时不怎么起眼的消旋抑制剂也随之“出圈”,收获了不少关注度。本文在此简单介绍一下这个小众产品。
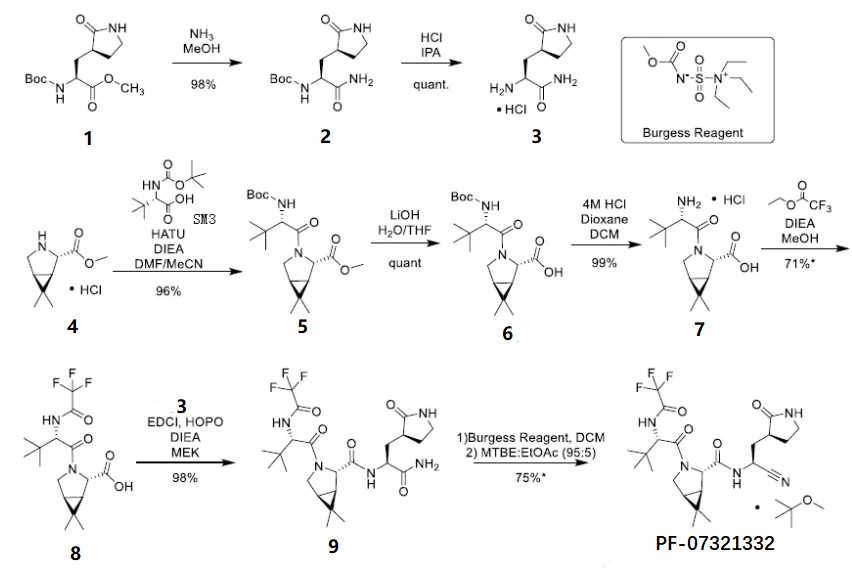
图1 PF-07321332合成路线
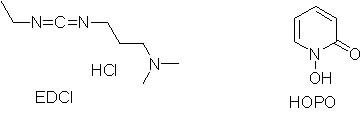
图2 EDCl与HOPO
众所周知碳二亚胺缩合剂是最早开发,也是最常用的一类缩合试剂。自从Sheehan 等人于1955 年开发了第一个碳二亚胺型缩合剂——N,N'-二环己基碳二亚胺(DCC) 以来[2],化学家们设计开发出一系列新型碳二亚胺类缩合剂,例如 N,N'-二异丙基碳二亚胺(DIC)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDCI)等。然而,碳二亚胺型缩合剂在活化 α-氨基酸时,由于其活性过高往往会导致氨基酸 α-位的手性中心发生一定程度的消旋。为了抑制外消旋化副反应的发生,化学家开发了一系列消旋抑制剂并将其与碳二亚胺型缩合剂联合使用。消旋抑制剂不仅能够在一定程度上抑制消旋,而且能够减少其它副反应的发生,使肽键形成的效率得以较大幅度的提升。目前,常见的消旋抑制剂包括:HOSu,HOBT,HOAT等十余种(图3)。其中最常用的是HOBT与HOAT。
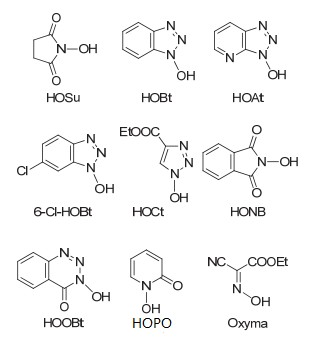
图3
在大多数文献报道中,碳二亚胺缩合试剂经常与HOBT或HOAT搭配使用。例如Carpino等学者在一篇文献中研究了DIC在是否添加消旋抑制试剂情况下的性能比较[3]。作者研究了利用固相合成法研究了一个多肽——ACP(65-74)的产率以及杂质情况(表1)。研究显示在不加HOAT或HOBT的情况下, DIC的缩合效果很差,产物收率只14%,当添加HOAT或HOBT后收率显著提高。另外一篇文献中,作者利用四种缩合试剂分别合成三种多肽:Z-Gyl-Leu-Val-OBzl(10)、Z-Gyl-Val-Val-OBzl(11)、Z-Gyl-Phe-Val-OMe(12)。研究发现DCC在添加了HOBT后,消旋杂质显著降低(表2)[4]。
表1 不同缩合试剂制备多肽ACP(65-74)的效果
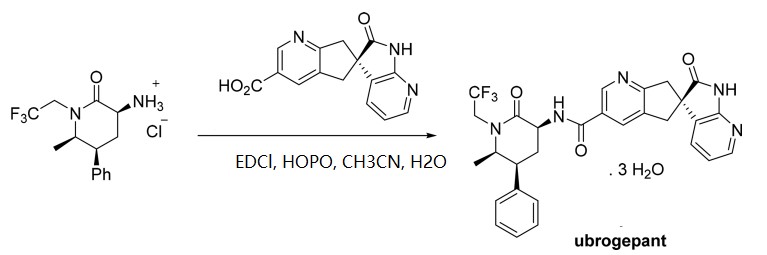
表2 不同缩合试剂制备多肽过程中的消旋杂质生成量对比
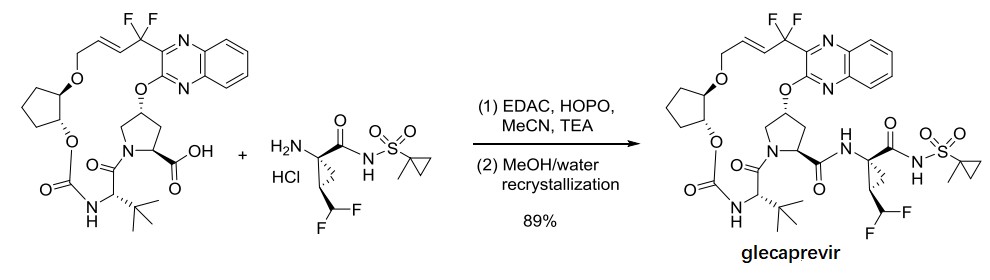
对于PF-07321332的合成,笔者没有找到关于HOPO与HOBT或HOAT的效果差异的相关研究。但是我们查阅了其他一些文献发现在某些肽键合成中,HOPO可能比HOBT或HOAT更有优势。例如,Yasuda等人在合成CGRP受体拮抗剂ubrogepant的时候采用了EDCl/HOPO的组合方式。作者指出,如果用HOBt会产生1%的消旋副产物,而使用HOPO则没有消旋副产物(图4)[5]。另外,David等人在合成glecaprevir的时候,也采用了EDCl/HOPO的组合方式[6]。作者发现在此条件下没有发现脯氨酸上的消旋异构体产生(图5)。另外,Young等人在生产一个API产品的时候也利用EDCl/HOPO的组合来合成肽键(图6)[7]。由此可见在某些情况下HOPO比常用的HOBT或HOAT更有优势,这也许是在PF-07321332合成中,化学家们使用HOPO的原因吧。
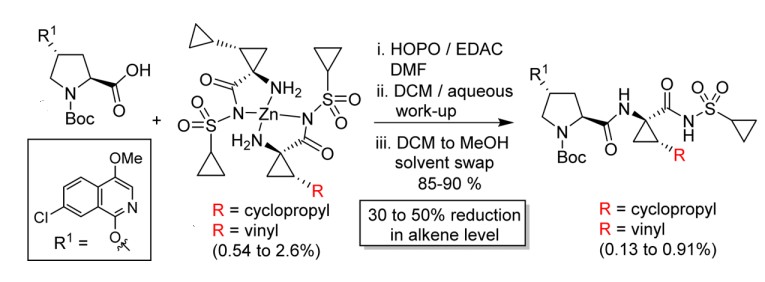
图4
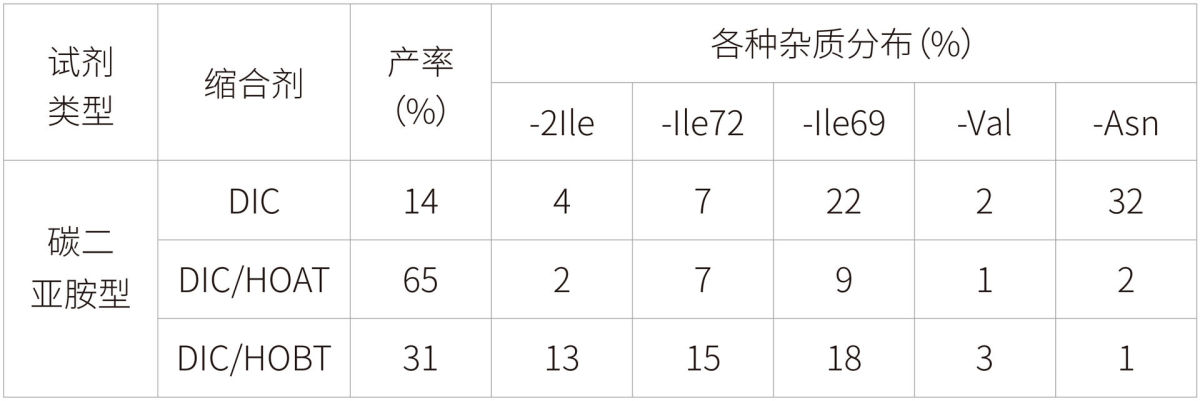
图5
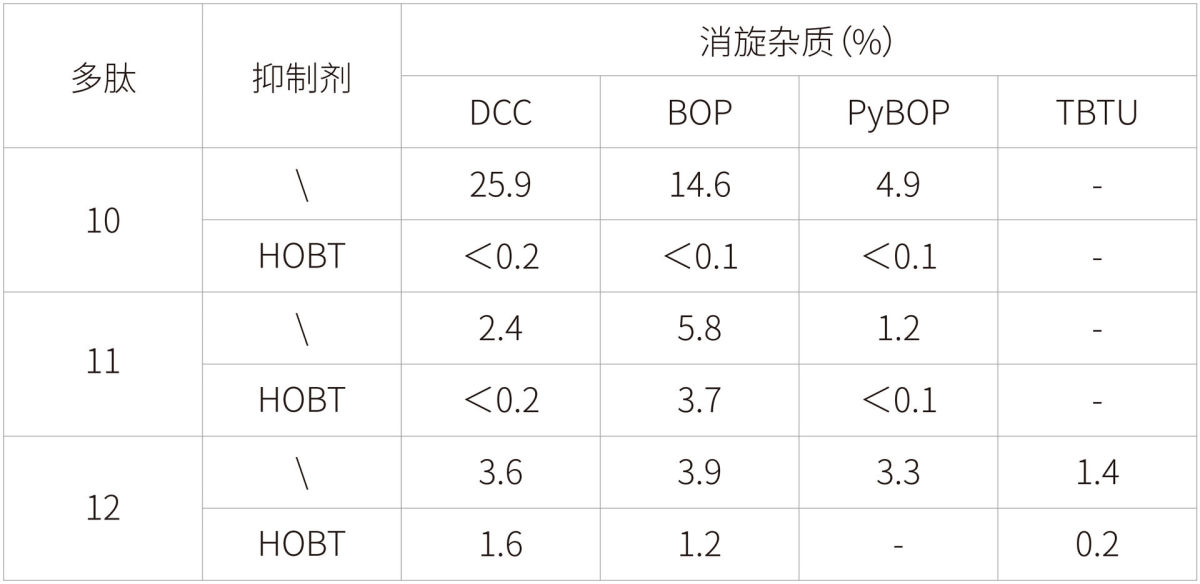
图6
HOPO是一种淡黄色结晶型粉末,熔点149-152℃。从安全性的角度看,HOPO是比HOBT或HOAT更加安全的化合物(HOBT 及其衍生物被认定为第一类爆炸物,其生产过程中的安全事故时有发生!)。昊帆生物致力于缩合试剂、保护试剂的研发与生产已近20年,积累了丰富的经验并形成了自己的特色。目前,我们能够生产包括HOPO在内的几乎所有的消旋抑制试剂。我们生产的HOPO在各项质量指标上处于行业领先水平,欢迎有需求的朋友来电咨询!
参考文献
[1] Owen, D. R.; Allerton, C. M. N.; Aanderson, A. S.; et al. Science, 2021: 374, 1586.
[2] Sheehan, J. C.; Hess, G. P. J. Am. Chem. Soc. 1955, 77, 1067.
[3] Carpino; L. A.; El-Faham, A.; Minor, C. A.; et al. J. Chem. Soc., Chem. Commun., 1994,201.
[4] Alericio, F.; et al. SYNTHESIS OF PEPTIDES AND PEPTIDOMIMETICS. Methods of Organic Chemistry.
[5] Yasuda, N.; Cleator, E.; Kosjek, B.; et al. Org. Process Res. Dev. 2017, 21, 1851.
[6] Hill, D. R.; Abrahamson, M. J.; Lukin, K. A.; et al. Org. Process Res. Dev. 2020, 24, 1393.
[7] Young, I. S.; Qiu, Y.; Smith, M. J. et al. Org. Process Res. Dev. 2016, 20, 2108.

