新闻动态
酰胺键是多肽药物、小分子药物和功能材料中无处不在的关键结构单元。此前,我们为大家介绍了多篇关于胺类化合物和羧酸进行酰胺化反应的相关研究,为酸胺缩合提供了丰富的合成思路。今天,我们将视角转向一条新的途径, Batra, S.团队报道了一种新的酰胺合成方法,能够实现硝基化合物(或亚硝基化合物)与芳基α-酮羧酸一步直接反应制备酰胺。
这项研究亮点在于:它展示了一种在水性介质中,无需过渡金属和还原剂参与,直接一步合成酰胺的创新方法,操作简便且条件温和。这项技术底物适用范围广,环境友好,为酰胺类化合物的绿色合成提供了新选择。
传统方法中,用硝基化合物合成酰胺,通常需要先将硝基还原为氨基,然后再与活化后的羧酸或者在缩合试剂作用下进行酰胺化反应。这个思路不仅步骤繁琐,还容易产生副产物。
Batra, S.团队则是另辟蹊径,巧妙的利用自由基机制,实现了硝基化合物(或亚硝基化合物)的直接酰胺化。其核心在于,利用过硫酸钾在碱性水溶液中产生硫酸根自由基,夺取芳基α-酮羧酸中的氢原子,脱羧生成关键的苯甲酰自由基,从而实现酰胺键的构建。
在Batra, S.团队的研究下,反应条件需在含水体系下进行,且引发剂和碱必须为含钾盐,最佳反应条件为:以乙腈/水(1:1)为溶剂,碳酸钾(1.5当量)为碱,过硫酸钾(3.0当量)为引发剂,硝基化合物(或亚硝基化合物,1.0 当量)和芳基α-酮羧酸(2.1 当量),在80°C下反应得到相应酰胺。另外,研究发现,反应的顺利进行高度依赖于钾盐的使用。
此方案展现出良好的底物适用性,适用于以下几类底物。
无论芳环上带有给电子基(如甲基)还是吸电子基(如氰基),反应都能顺利进行,以优异的收率得到相应的酰胺产物。多种取代的芳基α-酮羧酸同样能很好的参与反应。
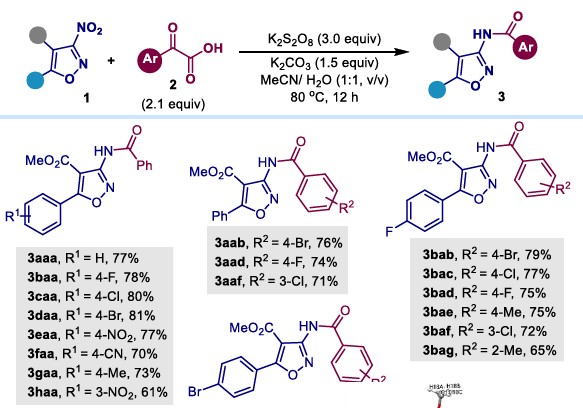
但是,异噁唑类底物4号位必须有吸电子基团才能实现转化,对于无取代等情况无法实现酰胺化。
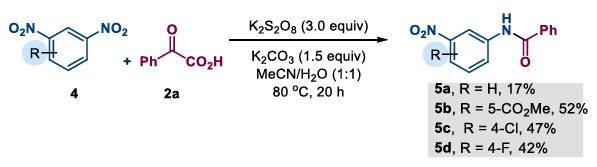
该团队也探索了部分1,3-二硝基苯及其衍生物的酰胺化反应,以17-52%的收率获得相应的N-(3-硝基苯基)苯甲酰胺产物,该方法为多硝基化合物的直接衍生化提供了一条新的路线。
基于对机理的深入理解,研究者成功将这一策略拓展至亚硝基化合物。亚硝基化合物与芳基α-酮羧酸在相同条件下,以中等偏上的收率直接得到一系列结构多样的酰胺。该转化适用于多种取代的亚硝基芳烃、杂环亚硝基化合物以及脂肪族亚硝基化合物。
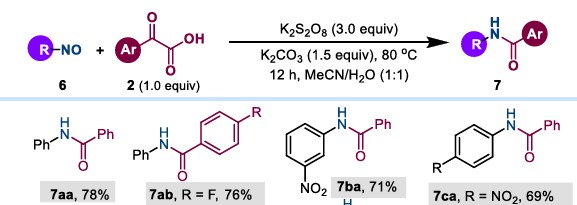
更有趣的是,研究发现,在水溶液中,N-苯甲酰基苯基羟胺在过硫酸钾存在下,无需碱参与,也能直接转化为酰胺。也就是说,只要反应底物的结构符合机理中的某一阶段,均可以通过此方案实现酰胺的合成。
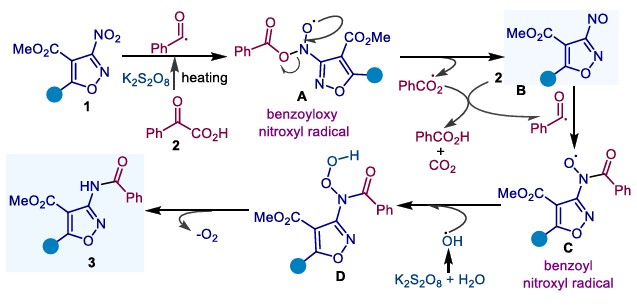
该团队提出的反应机理如下:以3-硝基异噁唑类底物为例,首先,在高温的碱性环境下,过硫酸钾分解生成硫酸根自由基,继而夺取芳基α-酮羧酸的氢原子并脱羧生成苯甲酰自由基。随后,该自由基进攻硝基芳烃中的硝基,夺取一个氧原子,生成苯甲酰氧自由基和亚硝基芳烃中间体,苯甲酰氧自由基与另一分子芳基α-酮羧酸反应重新生成苯甲酰自由基。紧接着,第二个苯甲酰自由基与亚硝基芳烃结合,形成苯甲酰亚硝基自由基中间体。 最后,该自由基与体系内产生的羟基自由基结合,经脱氧过程,最终生成目标酰胺产物。
总而言之,这项研究发展了一种条件温和、操作简便、无需过渡金属和还原剂参与、绿色环保的直接酰胺化方法。利用自由基转化过程,成功实现了3-硝基异噁唑类、1,3-二硝基苯类以及亚硝基化合物到酰胺的高效、绿色转化,为相关酰胺类化合物的合成提供了具有吸引力的新途径,也为绿色合成化学领域提供了重要的理论依据和实践案例。
苏州昊帆生物股份有限公司(股票代码:301393.SZ),成立于2003年,总部位于苏州市高新区,是一家为全球医药研发及生产企业提供特色原料的国家高新技术企业。产品主要应用于多肽、核苷酸和医药合成等领域,产品范围涵盖特色酰胺键构成用缩合剂、保护剂、链接剂、抗体偶联药物用蛋白质交联剂、分子砌块、脂质体、磷试剂等种类。目前已累计研发生产各类产品达1500多种。
经过二十余年的不懈努力和积累,昊帆生物在全球多肽合成试剂领域持续深耕,现已发展成为具有广泛定制产品覆盖能力和显著规模化生产优势的领先企业,可以满足各类客户的特定需求。我们诚挚邀请对该产品感兴趣的客户与我们联系,以便进一步了解产品详情,并探讨合作机会。
参考文献:
[1] Decarboxylative/Oxidative Amidation of Aryl α‑Ketocarboxylic Acids with Nitroarenes and Nitroso Compounds in Aqueous Medium.
DOI: 10.1021/acs.orglett.0c03666

