新闻动态
酰胺键不仅是多肽分子的基础结构,更是众多天然产物和药物分子的核心结构单元。随着生物活性分子设计的日益复杂化,传统多肽合成策略中繁琐的保护-脱保护步骤已成为制约合成效率的瓶颈,既会增加合成路线长度,还可能会引起副反应、收率下降等问题。
近年来,未保护氨基酸直接缩合策略逐渐成为研究热点。该方法旨在简化合成流程,降低成本,提升原子经济性。在这一领域,Yamamoto, H.团队继前期开发的硅烷介导氨基酸之间直接缩合后,近期又将目光投向了有机金属试剂——三甲基铝(Me3Al),探索其在多肽合成中的应用。
三甲基铝是一种高活性的路易斯酸,具有较强的亲电性和甲基化能力。作为有机铝试剂,它能够参与多种类型反应,特别是在活化羧基,促进酰胺化反应方面展现出独特的优势。但是三甲基铝遇水反应且自然的特性,使其有一定的危险性,操作门槛较高。
在Yamamoto, H.团队研究三甲基铝介导多肽合成之前,已经有若干研究三甲基铝用于酰胺合成的相关工作。
1. 辉瑞研发团队曾报道利用三甲基铝促进无保护羧酸与胺类化合物的直接缩合,其作用机制是通过形成铝酸盐中间体实现酰胺键的构建。
在底物适用性研究中,以4-苯基苯甲酸为固定羧酸,与不同类型的胺类化合物进行酰胺化反应,在三甲基铝作用下,伯胺,仲胺以及芳香胺均以优异的收率获得目标酰胺。
进一步地,以4-苯基苄胺为固定胺组分,与不同种类的羧酸进行反应,发现芳香酸的活性普遍优于脂肪酸。
2. Martin, S. F.团队则开发了一种三甲基铝促进氨基酸酯与游离氨基酸反应构建肽键的方法。该方案以羧酸酯或N-保护氨基酸酯作为亲电试剂,与游离氨基酸或二肽直接偶联,收率良好,但在尝试继续延长肽链,合成三肽和四肽时,出现明显的消旋现象,限制了其在长肽合成中的应用。
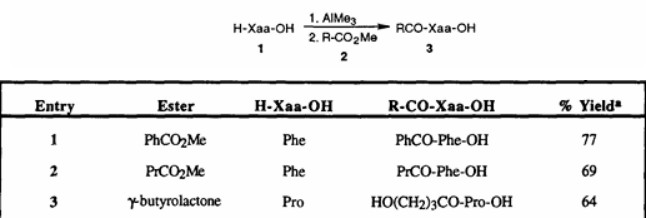
上述研究虽然验证了三甲基铝在酰胺化中的潜力和应用价值,但普遍在长肽链的合成中存在局限,难以满足复杂多肽结构的制备需求。
Yamamoto, H.团队提出了一种基于五元环机制的一锅法多肽合成策略,该方法充分发挥三甲基铝的多功能性,既活化羧基,又协调氨基亲核进攻,实现高效、高立体选择性的多肽合成。
1. 一锅法反应机制
其作用机制如下:首先,三甲基铝与游离氨基酸反应活化羧基,释放甲烷;随后与分子内氨基反应形成五元环中间体A,并释放第二分子甲烷;然后在另一分子三甲基铝催化下,新加入的氨基酸酯进攻中间体A发生开环反应,得到中间体B,最后经酸处理释放氨基,得到二肽产物。
若需继续延长肽链,在合成二肽的基础上,重复上述循环,或在最后一步引入Fmoc保护的氨基酰氯进行封端,从而精确控制肽链长度。
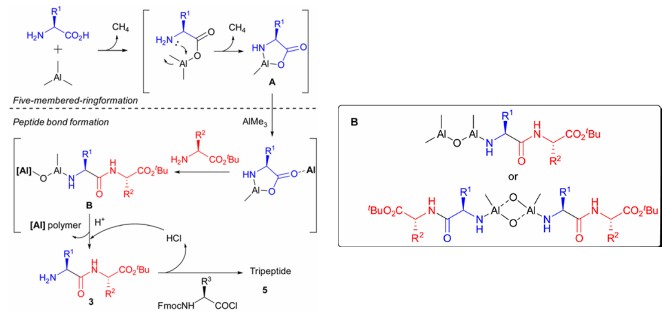
2. 反应条件优化
该团队以三肽合成为模型反应,进行反应条件探索,最终确定以二氯甲烷为溶剂,在低温(0℃)下预混游离氨基酸和三甲基铝以活化羧基,然后在室温下与氨基酸甲酯进行酰胺化反应,并以特戊酸进行酸处理,确保氨基完全游离,最后与Fmoc保护氨基酰氯反应得到三肽。
3. 优异的官能团兼容性和立体选择性
该合成策略展现出优异的官能团兼容性,对含有侧链的氨基酸,以及含有酯基、醚键、含硫氨基酸等均耐受,反应收率高,在整个合成过程中未观察到明显消旋化,立体选择性好。
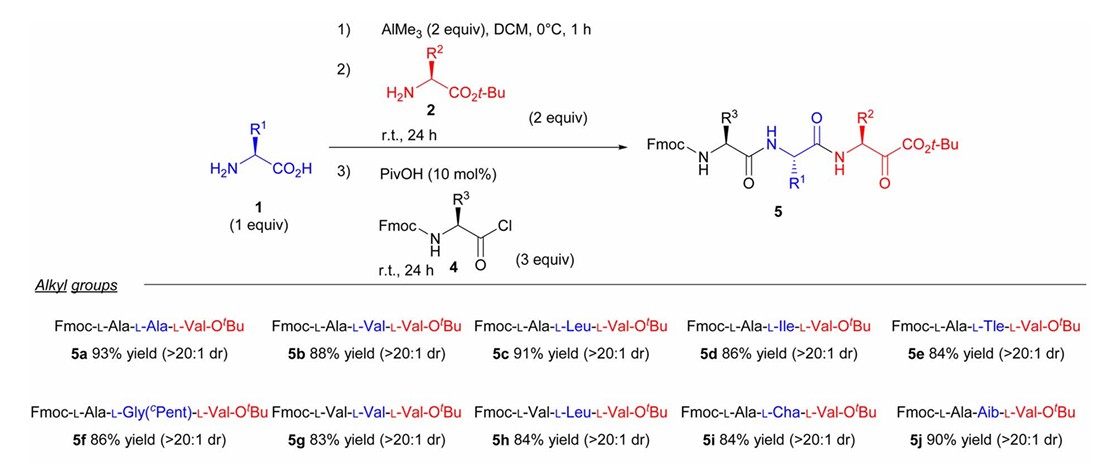
该团队在此基础上进一步探索了四肽和五肽的逐步合成,其合成收率维持在60%左右,展现出良好的扩展性。需要注意的是,研究发现合成肽链长度及收率受产物溶解度情况影响较大。
综上所述,三甲基铝是一个价廉易得,效率高,低消旋的缩合试剂。在使用过程中,无需进行预活化羧酸,显著减少合成步骤与试剂消耗,官能团兼容性好,在温和条件下为目标肽段的制备提供了便捷途径。这一突破性进展,为多肽药物和功能肽材料的合成领域提供了崭新的思路。
苏州昊帆生物股份有限公司(股票代码:301393.SZ),成立于2003年,总部位于苏州市高新区,是一家为全球医药研发及生产企业提供特色原料的国家高新技术企业。产品主要应用于多肽、核苷酸和医药合成等领域,产品范围涵盖特色酰胺键构成用缩合剂、保护剂、链接剂、抗体偶联药物用蛋白质交联剂、分子砌块、脂质体、磷试剂等种类。目前已累计研发生产各类产品达1500多种。
经过二十余年的不懈努力和积累,昊帆生物在全球多肽合成试剂领域持续深耕,现已发展成为具有广泛定制产品覆盖能力和显著规模化生产优势的领先企业,可以满足各类客户的特定需求。我们诚挚邀请对该产品感兴趣的客户与我们联系,以便进一步了解产品详情,并探讨合作机会。
参考文献:
[1] Trimethylaluminium-Facilitated Direct Amidation of Carboxylic Acids.
DOI: 10.1055/s-0030-1260982
[2] Application of AlMe3-mediated amidation reactions to solution phase peptide synthesis.
DOI: 10.1016/s0040-4039(98)00071-9
[3] Trimethylaluminum-mediated one-pot peptide elongation.
DOI: 10.1039/d3sc00208j

